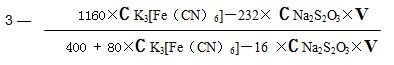蓝色氧化钨氧指数测定方法

1.1 基本原理
蓝钨中氧指数的测定,是基于它能溶解于氢氧化钾和一定量的铁氰化钾溶液,生成的钨酸钾(K2WO4),过量的铁氰化钾在酸性溶液中与碘化钾作用,并释放出碘,然后用硫代硫酸钠标准溶液滴定,从而计算出蓝钨中的氧指数。 其主要反应方程式如下:
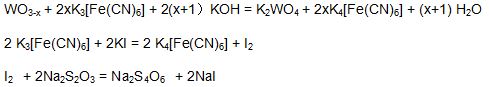
1.2 试剂
⑴氢氧化钾,分析纯,10g/100ml;
⑵盐酸,分析纯,1+1;
⑶碘化钾,分析纯,10g/100ml;
⑷硫酸锌,分析纯,10g/100ml;
⑸淀粉,分析纯,1g/100ml;
⑹重铬酸钾标准溶液:准确称取2.4515g经140~150℃烘干2h的基准重铬酸钾溶解于水,移入1000ml容量瓶中,用水稀释至刻度,混匀。此标准溶液的浓度为0.05mol/L。
⑺硫代硫酸钠标准溶液:称取12.5g硫代硫酸钠溶解于经煮沸并冷却至室温的水中,加0.1g碳酸钠,充分混匀,过滤于1000ml棕色容量瓶中,用水稀释至刻度,混匀,放置一星期后进行标定。此溶液每毫升约为0.05mol/L。
标定:准确量取20.00ml、0.05mol/L的重铬酸钾标准溶液于250 ml的三角瓶中,加入20 ml(1+1)盐酸,20 ml碘化钾溶液,混匀,放置5min后,用硫代硫酸钠标准溶液滴定至溶液呈淡棕色,再加入1 ml淀粉溶液,继续滴定至溶液蓝色消失为终点,所消耗硫代硫酸钠标准溶液的体积为V0ml,其化学反应如下:
3 Na2S2O3 + K2Cr2O7 + 6HCl = 2 Cr(OH)SO4 + 4 NaCl + 3S + 2H2O + KCl + Na2SO4
按下式计算硫代硫酸钠标液的摩尔浓度:
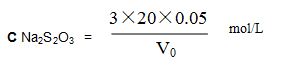
⑻铁氰化钾标准溶液:称取66.0克分析纯铁氰化钾于250 ml烧杯中,加水溶解后,移入1000ml容量瓶中,用水稀释至刻度,混匀,此溶液每毫升约为0.02mol/L。
标定:准确量取5.00ml铁氰化钾标准溶液于250 ml三角瓶中,加入20 ml(1+1)盐酸、20 ml碘化钾溶液,混匀,放置5min后,加入 20 ml硫酸锌溶液,用0.05mol/L的硫代硫酸钠标液滴定至淡棕色,再加入1 ml淀粉溶液,继续滴定至溶液蓝色消失为终点。所消耗硫代硫酸钠标准溶液的体积为V1ml,计算铁氰化钾标准溶液的摩尔浓度:
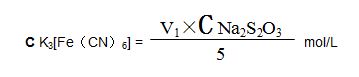
2.1 分析方法
准确称取0.2000克试样于250 ml三角瓶中,加入5.00ml铁氰化钾标准溶液,15ml氢氧化钾溶液,用少量水吹洗瓶壁,在低温处(约70℃)加热溶解15min,待试样完全溶解后取下,用水冷却至室温。加入20 ml(1+1)盐酸,20 ml碘化钾溶液,混匀后,放置5min后,用0.05mol/L的硫代硫酸钠标液,滴定至淡棕色,再加入1 ml淀粉溶液,继续滴定至溶液蓝色消失为终点。计下所消耗硫代硫酸钠标准溶液的体积为Vml。
2.2 氧指数计算方法
综上所有反应式及测定数据,所计算得蓝钨氧指数: