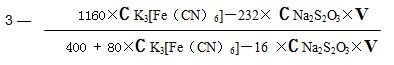Метод определения индекса оксида синего вольфрама

1.Principle
Проверка кислородного индекса оксида синего вольфрама основана на его растворимости в растворе гидроокиси калия и калия феррицианида, калиевой вольфрамовой кислоты (K2WO4). Передозированный раствор феррицианида калия вступит в реакцию с йодом калия в кислом растворе, иод высвободится. Титровать стандартным раствором тиосульфата натрия для расчета синего кислородного индекса оксида вольфрама.
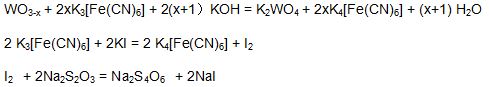
2.Агент
(1) Гидроксид калия, аналитическая чистота, 10 г / 100 мл.
(2) Соляная кислота, аналитическая чистота, 1 + 1.
(3) Йодид калия, аналитическая чистота, 10 г / 100 мл.
(4) Сульфат цинка, аналитическая чистота, 10 г / 100 мл.
(5) Крахмал аналитического качества, 1 г / 100 мл.
(6) Титрант бихромата калия: взвесить 2,4515 г и высушить его при температуре 140-150 ℃, растворить в воде, поместить в мерную колбу объемом 1000 мл, развести по весу, перемешать. Концентрация 0,05 моль / л.
(7) Стандартный раствор тиосульфата натрия: взвесить 12,5 г стандартного раствора тиосульфата натрия и растворить в воде, добавить 0,1 г соды, перемешать, профильтровать в коричневой бутылке объемом 1000 мл, разбавить водой и поставить на неделю для стандартизации. Концентрация составляет 0,05 моль / л.
Стандартизация: взвесить 20 мл, 0,05 моль / л стандартного раствора бихрома в 250 мл треугольной колбе, добавить 20 мл HCl, 20 мл раствора йода-калия, перемешать, поставить на 5 минут, наклонить раствором тиосульфата натрия, пока он не станет светло-коричневым, добавить 1 мл раствора крахмала, продолжайте наклонять, пока синий цвет раствора не исчезнет. Объем раствора тиосульфата натрия V0мл, химическая реакция:
3 Na 2 S 2 O 3 + K 2 Cr 2 O 7 + 6HCl = 2 Cr (OH) SO 4 + 4 NaCl + 3S + 2H 2 O + KCl + Na 2 SO 4
Рассчитать молярный раствор тиосульфата натрия :
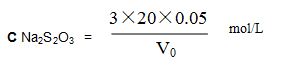
(8) Стандартный раствор феррицианида калия: взвесить 66 г аналитического стандартного раствора феррицианида калия в колбе на 250 мл, добавить воду и растворить, поместить в бутылку на 1000 мл, добавить воду и разбавить, перемешать, концентрация составляет 0,02 моль /. L.
Стандартизация: взвесить 5 мл стандартного раствора феррицианида калия в 250 мл треугольной бутылке, добавить 20 мл HCl, 20 мл раствора йода и калия, перемешать, поставить на 5 минут, наклонить раствором тиосульфата натрия до светло-коричневого цвета, добавить 1 мл раствора крахмала, наклонять до синего цвета цвет раствора исчезает. Объем раствора тиосульфата натрия V1мл, рассчитать молярную концентрацию стандартного раствора феррицианида калия:
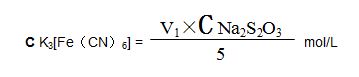
2. Метод анализа
Отвесить 0,2 грамма образца в 250 мл треугольной бутылке, добавить 5 мл стандартного раствора феррицианида калия, 15 мл раствора гидроксида калия, взорвать и очистить стенку бутылки, нагреть и растворить в течение 15 минут при температуре 70 70 до полного растворения образца, охладить до комнатной температуры. Добавьте 20 мл соляной кислоты, 20 мл раствора йодида калия, смешайте их и оставьте на 5 минут, наклоняйте 0,05 моль / л раствора тиосульфата натрия до тех пор, пока он не станет светло-коричневым, добавьте 1 мл раствора крахмала, продолжайте наклонять до исчезновения синего цвета раствора. Объем раствора тиосульфата натрия Vml.
2.1 Расчет индекса кислорода: